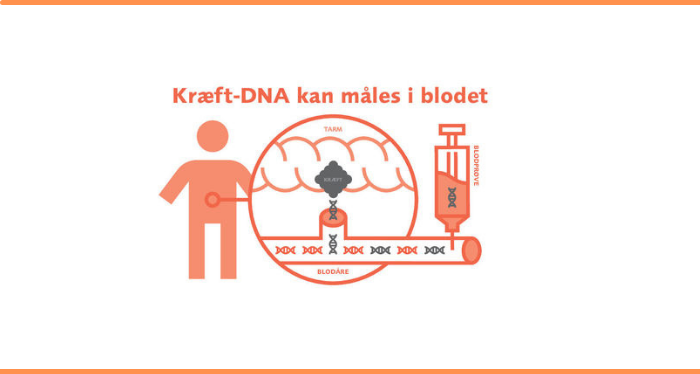
Beskrivelse af ctDNA metoden ved tarmkræft. Foto: cancer.dk
19-11-21
Cirkulerende kræft-DNA (ctDNA) er den hidtil stærkeste metode til at opdage tilbagefald ved kræftsygdom – den sætter os i stand til at opdage kræft tidligere, behandle målrettet og undgå at give kemoterapi eller anden medicinsk kræftbehandling til raske patienter. Ledelsen i det nationale forskningscenter på området tror så meget på metoden, at alle forskningsstudier fra start både skal indeholde en sundhedsøkonomisk vurdering og have deltagelse fra hele landet. Det vil nemlig gøre den endelige implementering langt nemmere og hurtigere – til gavn for både patienter og samfundsøkonomi.
Som leder af DCCC Dansk Forskningscenter for cirkulerende tumor DNA guided kræftbehandling har man ansvaret for lidt af et guldæg. CtDNA er den stærkeste risikomarkør for tilbagefald man har set til dato – og har dermed potentiale til at skabe enorme fremskridt på kræftområdet. Derfor har Claus Lindbjerg Andersen og Lars Dyrskjøt Andersen, der udgør ledelsen i det nationale forskningscenter, en klar plan for, hvordan metoden hurtigst muligt kan komme ud og gøre gavn for kræftpatienter i Danmark.
”Vi har fundet og testet biomarkører for forskellige kræfttyper i prospektive studier og er derfor ikke i tvivl om, at vi kan vinde meget ved at bruge den her metode. Vi fokuserer nu på at lave interventionsstudier for at bekræfte og dokumentere den kliniske effekt,” siger Lars Dyrskjøt Andersen.
Centeret danner rammerne for en lang række forskningsprojekter, der alle centrerer sig om ctDNA-analyse som metode, men de mange studier har også andre – og lidt særlige – ting til fælles.
”Vi tror på, at den her nye diagnostiske test er så god, at den skal implementeres i det danske sundhedsvæsen. Derfor bygger vi en 360 graders analyse ind i vores studier, hvor vi blandt andet ser på de sundhedsøkonomiske aspekter ved at anvende metoden og patienternes livskvalitet,” siger Claus Lindbjerg Andersen.
Pointen med, at alle studierne indeholder de elementer er, at centerets forskning kan udgøre det grundlag, som sundhedsvæsnets beslutningstagere skal bruge for at vurdere, om metoden skal tilbydes i det danske sundhedssystem.
”Samtidig er alle vores studier nationale. De udspringer typisk fra universitetshospitalerne, men det er meget vigtigt at have regionshospitalerne med også. De kan dels styrke rekrutteringen af patienterne til de forskellige studier, og dels betyder deres deltagelse, at flere sundhedsprofessionelle bliver trygge ved metoden. Det vil i sidste ende gøre det langt nemmere at implementere brugen af ctDNA i hele landet, når vi er klar til det,” siger Claus Lindbjerg Andersen.
Opfølgning og behandling kan målrettes
Når troen på ctDNA som metode er stor, skyldes det naturligvis de resultater, metoden indtil nu har kastet af sig. Den vil ganske enkelt betyde, at vi kan opdage tilbagefald blandt kræftpatienter tidligere. Og tid er en af de allermest afgørende faktorer i kræftbehandling.
”Vi er i stand til at opdage tilbagefald langt tidligere end ved CT-skanninger, som typisk er den nuværende metode til opfølgning efter kræftsygdom. Det betyder, at vi kan starte behandlingen ved tilbagefald, før kræften vokser for meget og spreder sig. Vi har en klar forventning om, at det vil have en positiv effekt,” siger Lars Dyrskjøt Andersen.
Oven i den tidligere indsats ved tilbagefald kommer, at de kræftpatienter, der ikke oplever tilbagefald kan slippe for den kemoterapi eller anden medicinsk behandling, man i nogle tilfælde giver alle patienter forebyggende.
”Fordi kræft er så alvorlig en sygdom, accepterer vi, at der er en del bivirkninger ved kemoterapi. Det giver god mening for patienter med kræft, men som det er i dag, bruger vi i flere behandlinger kemoterapi eller eksempelvis immunterapi som en slags one size fits all-forebyggende behandling. Vores håb er, at vi fremover kun behøver at give medicinsk kræftbehandling til dem, der rent faktisk har kræft-DNA i blodet. Det vil spare en masse patienter for bivirkningerne fra behandlingen, og vi kan bruge ressourcerne langt bedre,” siger Lars Dyrskjøt Andersen.
Samtidig bliver det muligt at overvåge kræftens udvikling og reaktion på eksempelvis kemoterapi. Det giver lægerne mulighed for at målrette behandlingen efter højest mulig effekt med færrest muligt bivirkninger.
Centeret skal få metoden ud på sygehuse i hele landet
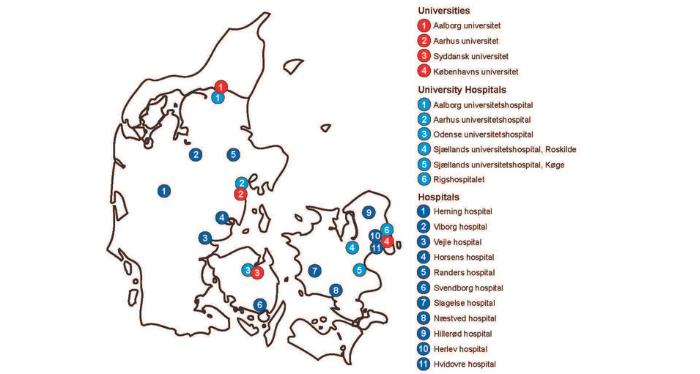
Deltagende institutioner i det nationale ctDNA forskningscenter: Som indikeret på figuren, er der deltagende institutioner (universiteter og hospitaler) fra hele Danmark, samt alle afdelinger ansvarlige for behandling af kræftpatienter (kirurgi, patologi, onkologi, radiologi, nuklearmedicin, genomisk medicin og molekylærmedicin.)
Analyse af ctDNA er en højteknologisk metode, der både kræver særligt udstyr og særlige kompetencer – blandt andet i at tage blodprøverne rigtigt. Det kunne tale for en høj specialisering på få hospitaler. Men det strider mod ambitionen om at generere hurtig viden og lade metoden komme mange patienter til gavn. I stedet stilles viden og infrastrukturer til rådighed, så også mindre hospitaler har mulighed for at deltage.
”Det er ikke sådan, at vi forestiller os, at de mindre hospitaler nødvendigvis skal starte store kliniske studier på det her område, men det er vigtigt for os, at de har muligheden for det, og særligt vigtigt er det at sørge for, at de har mulighed for at deltage i de forsøg, vi kører. Det giver patienterne mulighed for at være med i opfølgningsprogrammer med ctDNA og samtidig kan vi hurtigere få nok patienter med i studierne, så vi hurtigere kan etablere den nødvendige viden,” siger Lars Dyrskjøt Andersen.
Samtidig er udbredelsen til flere hospitaler – også de mindre af slagsen – med til at gøre flere forskere og læger fortrolige med metoden. Lever metoden op til forventningerne, vil det være en stor fordel, når den skal implementeres over hele landet.
”Det er vigtigt for os at få hele landet med til at prøve metoden af på kræftpatienter. Den nationale udbredelse skal både sikre, at patienter i hele landet har samme mulighed for at blive diagnosticeret og fulgt op med de nyeste metoder og samtidig bidrage til, at det er nemt at implementere metoden på sygehuse over hele Danmark, når vi bliver klar til det,” siger Claus Lindbjerg Andersen.
Med flere end 160 læger og forskere fra fire universiteter og 17 hospitaler, der samlet dækker de fem regioner, er den nationale udbredelse faktisk allerede en realitet.
”De 25 millioner fra Knæk Cancer til at oprette og drive det her som et nationalt forskningscenter betyder, at vi er kommet rigtig godt fra start. Vi har naturligvis fokus på at få sat flere studier i gang, men har samtidig overskud til at sikre, at vi får metoden bredt ud til hele landet og får samlet den nødvendige viden, der endegyldigt vil slå fast, om den her metode er det markante fremskridt, som alt lige nu tyder på,” siger Claus Lindbjerg Andersen.
Mandag og tirsdag den 22. og 23. november holder det nationale ctDNA-forskningscenter årsmøde i Odense. Tilmelding er ikke længere mulig, men du kan orientere dig i programmet her.
Status på forskning i ctDNA
Den igangværende forskning i centeret spænder over retrospektive studier, prospektive studier og helt til interventionsstudier. Centeret stiller viden og infrastrukturer til rådighed for deltagerne, hvilket skal gøre det nemmere at igangsætte interventionsstudier for flere kræftsygdomme. Herunder kan du se, hvilket forskningsstadie forskellige kræftformer lige nu befinder sig i.
Igangværende retrospektive og prospektive studier:
- Hudkræft
- Kræft i spiserøret
- Lungekræft
- Sarkomer
Planlagte interventionsstudier med opstart i 2022
- Analkræft
- Kræft i bugsputkirtlen
Igangværende interventionsstudier
- Blærekræft
- Tarmkræft
